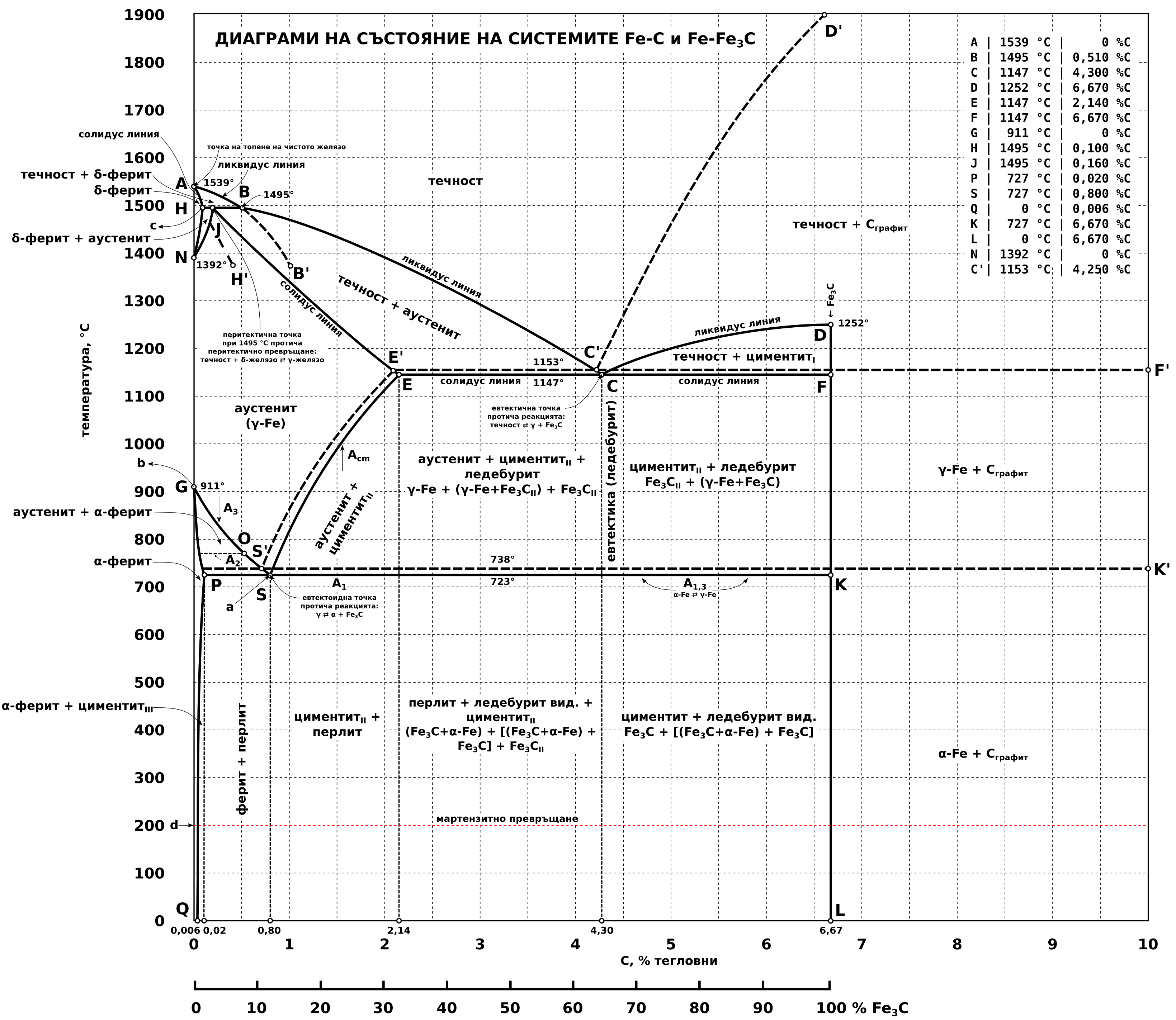
Фазовая диаграмма системы Fe–C
Фазовая диаграмма (или диаграмма фазового равновесия) системы железо-углерод представляет собой графическое изображение фазового состояния сплавов железо-углерод в зависимости от их химического состава и температуры.
История (Часть 1)
Началом изучения диаграммы состояния системы железо-углерод и процессов термической обработки железо-углеродистых сплавов можно считать 1868 год, когда русский ученый Дмитрий Чернов опубликовал свои исследования сталей, используемых преимущественно для изготовления орудий. Этот же год можно считать годом зарождения металлургии как науки, поскольку именно тогда были впервые обнаружены структурные изменения, происходящие в железоуглеродистых сплавах.
В этом исследовании Чернов впервые указал на существование критических точек [1] в состоянии стали, а также доказал их зависимость от содержания в ней углерода, тем самым впервые дав представление о диаграмме состояния системы железо-углерод.
Критические точки:
- точка а (~700 °C) — минимальная температура закалки стали;
- точка b (~900 °C) — температура изменения структуры стали;
- точка c — температура плавления сталей;
- точка d (~200 °C) — температура мартенситного превращения.
История (Часть 2)
Наиболее важные исследования, приведшие к окончательному построению фазовой диаграммы системы железо-углерод, были проведены в последней четверти XIX века. Положение критических точек на этой диаграмме Чернов определял на глаз, оценивая их по цвету закаленной стали. Известный французский исследователь Флорис Осмонд с помощью пирометра, изобретенного Анри Луи Ле Шателье, более точно определил положение критических точек на диаграмме, описал характер микроструктурных изменений, происходящих в стали при прохождении ею этих критических точек, и дал названия основным структурным фазам железоуглеродистых сплавов.
Образование твердых растворов при нагревании сплавов железа с углеродом было замечено английским ученым Уильямом Чандлером Робертсом-Остином и доказано с помощью прямого металлографического анализа французским ученым Ле Шателье и русскими учеными А. А. Байков и Н. Т. Гудцов. Используя данные этих исследований и теорию фазовых переходов, разработанную американским ученым Уиллардом Гиббсом, ученые Х. Розебом и Робертс-Остин представляют первый вариант фазовой диаграммы, которая из-за неполноты использованных данных не отличается большой точностью и полнотой. Лишь в конце XIX века немецкий ученый П. Херенс, используя опыт, накопленный его предшественниками, создал и опубликовал диаграмму, достаточно близкую к современной.
С совершенствованием методов исследования в последующие годы в схеме, созданной П. Херенсом, были сделаны существенные, но не принципиально отличающиеся разъяснения. Фактически изучение фазовой диаграммы системы железо-углерод продолжается, хотя кардинальных изменений в ее облике не ожидается.
Компоненты системы железо-углерод
Аллотропные формы железа
- α-Fe (α-железо) – ОЦК-решетка, a = 2,86 Å, ниже 910 °C;
- γ-Fe (γ-железо) – СКЦ-решетка, a = 3,65 Å, 911–1403 °C;
- Аллотропная форма α-Fe существует в двух диапазонах: ниже 911 °C и 1392–1539 °C. Высокотемпературная форма α-Fe (δ-Fe) имеет решетку a = 2,93 Å.
Твёрдые растворы железа
Железо может образовывать твёрдые растворы замещения (с металлами) и внедрения (с C, N, H). Растворимость углерода в α-Fe < 0,02%, а в γ-Fe до 2,14%. В металлургии:
- феррит — твёрдый раствор в α-железе,
- аустенит — твёрдый раствор в γ-железе.
Цементит
Химическое соединение углерода с железом (Fe3C). Состав: 75% Fe, 25% C (6,67% по массе), tпл ~1250 °C, высокотвёрдый (800 HB) и хрупкий. Может образовывать твёрдые растворы замещения и разлагаться с выделением графита.
Типы цементита:
- первичный, вторичный, третичный;
- эвтектический (в белых чугунах);
- эвтектоидный (часть перлита).
Диаграмма состояний
Фазовую диаграмму системы железо-углерод можно представить в двух вариантах: стабильная система Fe-C (графит) и метастабильная система – Fe-Fe3C. Метастабильная система Fe-Fe3C реализуется только при содержании углерода до 6,67% (масс.). Цементит имеет узкую область однородности, которая обычно изображается вертикально.
Диаграмма метастабильной системы Fe-Fe3C
Линия ABCD — ликвидус (выше только жидкая фаза). Линия AHJECF — солидус (ниже только твёрдая фаза). Между ними — сосуществование жидкой и твёрдой фаз.
Фазы в Fe-Fe3C:
- Жидкая фаза L (выше линии ABCD);
- Цементит Fe3C (линия DFKL);
- Феррит (α-Fe), Аустенит (γ-Fe), Графит (низкая плотность).
Три нонвариантные реакции
- Перитектическая (1495 °C): L + Feδ → Feγ.
- Эвтектическая (1147 °C): L → Feγ + Fe3C (ледебурит).
- Эвтектоидная (727 °C): Feγ → Feα + Fe3C (перлит).
Перлитное превращение происходит во всех сплавах с C > 0,02%.
Основные линии диаграммы:
- A1 — эвтектоидная T (нижняя граница аустенита);
- A3 — нижняя граница аустенита при низком C;
- Aсм — нижняя граница аустенита при высоком C;
- A2 — точка Кюри, 770 °C, ниже которой феррит ферромагнитен.
Диаграмма стабильной системы графита Fe-C

Пунктирными линиями показана часть, отличающаяся от метастабильной диаграммы Fe-Fe3C. Доэвтектическая область — ликвидус δ-Fe (AB) и γ-Fe (BC’), а сверхэвтектическая — ликвидус графита (C’D’). Экспериментально установлена до 2887 °C и 7,5% C (масс.) или 35% (атом.).
Эвтектическое превращение при 1153 °C:
L ⇄ Feγ + C (графит). Горизонтальная линия E’C’F’ расширена при C от 2,88% до 27% (масс.) или 65% (атом.) и экстраполирована до 100% графита. Эвтектика графита C’ содержит 4,25% (масс.) или 17,1% (атом.) C.
Кривая E’S’ показывает растворимость графита в аустените. При 738 °C и содержании 0,66% C (масс.) или 3% (атом.) образуется эвтектоид.
Источники
- А. П. Гуляев, Металлургия, учебник для вузов, 6-е издание, М., Металлургия, 1986, с. 141 – 160;
- Чернов, Дмитрий Константинович — биография (архив 2017-09-30);
- Эдкок Ф., Журнал Института железа и стали, т. 135, 1937, стр. 281 – 292;
- Бакли, Р. А. и Хьюм-Ротери У., Журнал Института железа и стали (L), т. 196, 1960, стр. 403 – 406;
- Диаграмма метастабильного состояния железо-углерод (Fe-C) // Вычислительная термодинамика (архив 2012-06-28);
- Доктор. Дмитрий Копелиович, «Фазовая диаграмма железо-углерод»;
- Ой. А. Банных и др., «Диаграммы состояния бинарных и многокомпонентных систем на основе железа». М.: Металлургия, 1986, с. 95 – 100;
- Эдкок, Ф., Журнал Института железа и стали, т. 137, стр. 281 – 192;
- Бенц М.Г. и Эллиот Дж.Ф., Труды AIME, т. 221, 1961, стр. 323 – 331;
- Биография Дмитрия Чернова (архив 2017-09-30).

Добавить комментарий